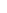PXSJ-226对硝酸根离子浓度测定的实验方法

2011-04-09
一 实验准备:
1.实验设备:PXSJ-226实验室离子计、JB-1磁力搅拌器、PNO3(01)硝酸根选择性电极、232(01)参比电极(甘汞电极)、T-820D温度。
2.实验溶液:配制硝酸钠溶液(0.1mol/L、0.01mol/L、0.001mol/L、0.0001mol/L)
3.硝酸钠(0.1mol/L)配制方法:取8.499g硝酸钠溶于烧杯中,在将其移入1000ml的容量瓶中,加蒸馏水至刻度即可。以下浓度的溶液则按逐步稀释法即可。
4.硝酸钠溶液配制方法:(0.01mol/L、0.001mol/L、0.0001mol/L)
用配制成0.1mol/L的硝酸钠溶液,按1:10浓度按逐步稀释的方法即可。
二 实验过程:
(1)实验前先将各电极在相对应的0.001mol/L的硝酸钠溶液中浸泡2小时,再用去离子水洗净待测。
(2)按照PXSJ-226说明书所说,装备好测试仪器">测试仪器,将待测溶液放入烧杯中,放置在磁力搅拌器上,打开电源,进行测试。现对各浓度下的硝酸钠的电位测试数据如下:
硝酸钠各浓度下的参考电位:
图中:C为硝酸根离子的浓度。
MV为测量溶液的电位。
从上图中可得出电位E与离子浓度的关系为一直线。
则可得到公式:E=klg[c]+b,其中E为所测电位,K为直线的斜率,C为离子浓度,b为直线在Y轴上的截距。根据实验数据,计算出k=-57,b=-17.5,代入原公式得:E=-57lg[c]-17.5。
假设某一未知溶液测得电位为100mv,代入上面的公式得:lg[c]=117.5/-57=-2.0614,从中可以计算出溶液中离子的浓度为0.00868mol/L。
注:为减少误差,用户在做测量或实验时,应该将溶液的温度偏差控制在相对一致的范围。在计算以上直线的斜率时可取溶液0.01mol/L和0.001mol/L这二点来计算斜率、截距或实际测量值相邻二点来计算斜率、截距,以减少计算误差
所有测试数据以人机对话方式操作,最终结果根据用户不同要求直接显示出来,以PX,mol/l,mmol/l,g/l,mg/l,ug/l等为单位。不需要用户手工计算。
1.开机显示时间,进入测量界面,选择离子名称,并确认。
2.进入测量界面,选择测量模式。(PX,PX直读浓度等6种模式)。
3.具体操作过程参照说明书及氟离子方法。
四.注意事项:
1..浓度范围:1×10-1~1×10-5mol/L No3-
2.该电极在搁置了较长时间后再使用时,应先放在1×10-3mol/L NaNO3溶液中浸泡数小时以上,再用去离子水洗净待测
3..测度时应在NaNO3标准液中加入离子强度调节剂NaH2PO4,使其本底溶液浓度为0.1mol/L NaH2PO4
4.该电极在使用时切忌将敏感膜与硬物碰撞,以免损坏电极。
最新资讯